Определение в 2020 г. пространственной структуры основной протеазы (MPro) SARS-CoV-2 – фермента, играющего чрезвычайно важную роль в жизненном цикле вируса, – создало предпосылки не только для понимания его функции и механизма действия, но и для разработки новых эффективных ингибиторов на основе прямых методов компьютерного конструирования лекарств, использующих данные о структуре молекулярной мишени. В частности, 25 марта 2020 г. в Банк данных белков была депонирована структура MPro SARS-CoV-2 в комплексе с молекулой X77 – мощным ингибитором как SARS-CoV, MERS-CoV, так и SARS-CoV-2. В связи с этим был осуществлен виртуальный скрининг потенциальных ингибиторов фермента, направленный на идентификацию соединений с фармакофорными свойствами ингибитора X77, выполнена in silico оценка их потенциальной анти-SARS-CoV-2 активности и идентифицированы молекулы, перспективные для создания новых эффективных препаратов для терапии COVID-19. Проведенные исследования включали следующие этапы (рис. 1):
1) построение модели фармакофора, описывающей совокупность структурно-функциональных свойств ингибитора X77, которые обеспечивают эффективность его взаимодействий с активным центром Mpro SARSCoV-2;
2) фармакофорный анализ 213,5 миллионов малых молекул из библиотек веб-сервера Pharmit (http://pharmit.csb.pitt.edu), позволяющего проводить интерактивное исследование химического пространства с целью поиска потенциальных лекарств на основе сходства фармакофорных моделей соединений с известными ингибиторами белковой мишени;
3) молекулярный докинг и молекулярную динамику отобранных соединений с MPro SARS-CoV-2;
4) расчет величин свободной энергии связывания с последующей идентификацией молекул, перспективных для разработки эффективных противовирусных препаратов.

Рис. 1. Схема алгоритма виртуального скрининга потенциальных ингибиторов MPro SARS-CoV-2
В результате реализации данного комплексного вычислительного подхода были обнаружены пять соединений, перспективных для синтеза и биомедицинского анализа. К сожалению, у авторов не было возможности провести синтез и тестирование найденных соединений на анти-SARS-CoV-2 активность за относительно небольшой промежуток времени. В связи с этим было принято решение использовать стратегию перепрофилирования лекарств, под которой понимается процесс определения новых терапевтических показаний для зарегистрированных ранее и доступных лекарственных препаратов. Для реализации данной стратегии была сформирована библиотека биологически активных молекул, которая включала 28 860 одобренных для применения в клинике препаратов и лекарственных веществ, находящихся на различных стадиях доклинических и клинических испытаний. Методами молекулярного моделирования проведен виртуальный скрининг созданной молекулярной библиотеки для обнаружения потенциальных ингибиторов консервативного домена HR1 белка S SARSCoV-2, играющего ключевую роль в слиянии мембран вируса и клетки хозяина. В результате анализа in silico были обнаружены девять молекул, способных согласно расчетным данным связываться с доменом HR1 SARS-CoV-2 и блокировать функциональную активность коронавируса. Биомедицинское тестирование этих молекул, проведенное в Университете Фудань (Шанхай, Китай), позволило обнаружить соединение-лидер − противоопухолевый препарат Навитоклакс (рис. 2), который проявляет высокую ингибиторную активность по отношению к различным штаммам SARS-CoV-2 и их вариантам, в том числе штаммам Дельта и Омикрон, а также к родственным коронавирусам SARS-CoV и MERS-CoV. На моделях in vitro показано, что Навитоклакс селективно связывается с доменом HR1 белка S, блокируя проникновение вируса в клетки хозяина. Кроме того, известно, что этот противоопухолевый препарат имеет много уникальных достоинств, включая низкую стоимость, хорошую пероральную биодоступность, экономичную технологию производства и всесторонне охарактеризованную безопасность in vivo. Поэтому он может быть быстро перепрофилирован и использован в качестве эффективного препарата против SARS-CoV-2 и других известных коронавирусов человека для клинического применения в ближайшем будущем.
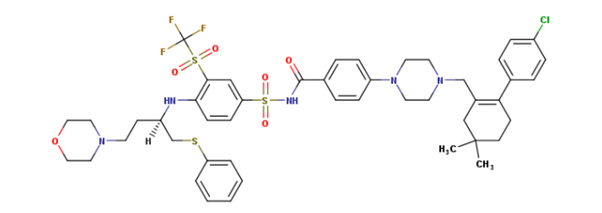
Рис. 2. Химическая структура Навитоклакса
В другом исследовании c использованием технологий искусственного интеллекта были разработаны две генеративные модели автоэнкодера для конструирования новых лекарственных веществ, способных ингибировать каталитическую активность MPro SARS-CoV-2. Разработана архитектура нейронной сети (рис. 3), сформирована виртуальная библиотека потенциальных ингибиторов фермента, выполнен виртуальный скрининг соединений из этой библиотеки и предсказаны значения свободной энергии связывания комплексов лиганд/MPro. Обучение нейронной сети и ее тестирование показали, что созданные модели автоэнкодера позволяют генерировать малые молекулы с высокой противовирусной активностью и приемлемыми фармакологическими свойствами. С помощью разработанной нейронной сети осуществлен de novo дизайн 95775 потенциальных ингибиторов MPro SARS-CoV-2 с последующей in silico оценкой их ингибиторной активности. В результате проведенных исследований отобраны семь соединений, которые характеризуются низкими значениями свободной энергии связывания, близкими к величинам, полученным с помощью идентичного вычислительного протокола для двух мощных ингибиторов MPro, использованных в расчетах в качестве позитивного контроля. Полученные результаты свидетельствуют о перспективности использования идентифицированных соединений в работах по созданию новых препаратов против COVID-19, терапевтическое действие которых основано на ингибировании ферментативной активности MPro SARS-CoV-2.
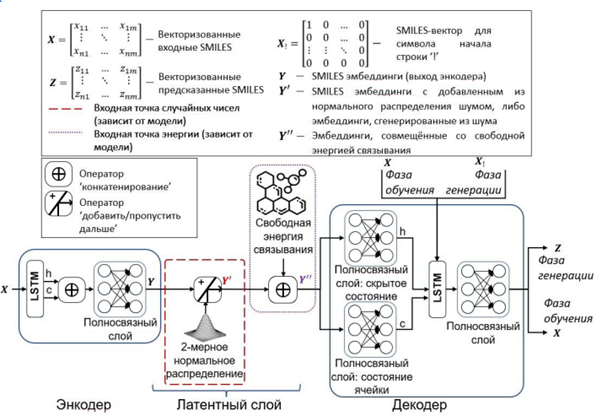
Рис. 3. Высокоуровневая архитектура моделей разработанной нейронной сети
Таким образом, в результате исследований, проведенных с помощью технологий молекулярного моделирования и глубокого обучения, авторами обнаружен набор лекарственных веществ, способных ингибировать функционально важные консервативные области белков SARS-CoV-2 и блокировать репликационный цикл вируса. Среди этих соединений следует особо выделить противоопухолевый препарат Навитоклакс, формирующий многообещающую базовую структуру для создания эффективного и безопасного перорального лекарственного средства широкого спектра действия против SARS-CoV-2 и других известных патогенных коронавирусов человека, а также их модификаций, которые могут появиться в будущем.